Ten eerste de structuur en eigenschappen van SiC-kristal.
SiC is een binaire verbinding gevormd door het Si-element en het C-element in een verhouding van 1:1, dat wil zeggen 50% silicium (Si) en 50% koolstof (C), en de structurele basiseenheid ervan is de SI-C-tetraëder.
Schematisch diagram van de structuur van de siliciumcarbide-tetraëder
Si-atomen hebben bijvoorbeeld een grote diameter, wat overeenkomt met een appel, en C-atomen hebben een kleine diameter, wat overeenkomt met een sinaasappel, en een gelijk aantal sinaasappels en appels zijn op elkaar gestapeld om een SiC-kristal te vormen.
SiC is een binaire verbinding, waarbij de atoomafstand van de Si-Si-binding 3,89 A is. Hoe kunnen we deze afstand begrijpen? Momenteel heeft de meest uitstekende lithografiemachine op de markt een lithografienauwkeurigheid van 3 nm, wat een afstand is van 30A, en de lithografienauwkeurigheid is 8 maal die van de atomaire afstand.
De Si-Si-bindingsenergie is 310 kJ/mol, dus je kunt begrijpen dat de bindingsenergie de kracht is die deze twee atomen uit elkaar trekt, en hoe groter de bindingsenergie, hoe groter de kracht die je nodig hebt om uit elkaar te trekken.
Si-atomen hebben bijvoorbeeld een grote diameter, wat overeenkomt met een appel, en C-atomen hebben een kleine diameter, wat overeenkomt met een sinaasappel, en een gelijk aantal sinaasappels en appels zijn op elkaar gestapeld om een SiC-kristal te vormen.
SiC is een binaire verbinding, waarbij de atoomafstand van de Si-Si-binding 3,89 A is. Hoe kunnen we deze afstand begrijpen? Momenteel heeft de meest uitstekende lithografiemachine op de markt een lithografienauwkeurigheid van 3 nm, wat een afstand is van 30A, en de lithografienauwkeurigheid is 8 maal die van de atomaire afstand.
De Si-Si-bindingsenergie is 310 kJ/mol, dus je kunt begrijpen dat de bindingsenergie de kracht is die deze twee atomen uit elkaar trekt, en hoe groter de bindingsenergie, hoe groter de kracht die je nodig hebt om uit elkaar te trekken.
Schematisch diagram van de structuur van de siliciumcarbide-tetraëder
Si-atomen hebben bijvoorbeeld een grote diameter, wat overeenkomt met een appel, en C-atomen hebben een kleine diameter, wat overeenkomt met een sinaasappel, en een gelijk aantal sinaasappels en appels zijn op elkaar gestapeld om een SiC-kristal te vormen.
SiC is een binaire verbinding, waarbij de atoomafstand van de Si-Si-binding 3,89 A is. Hoe kunnen we deze afstand begrijpen? Momenteel heeft de meest uitstekende lithografiemachine op de markt een lithografienauwkeurigheid van 3 nm, wat een afstand is van 30A, en de lithografienauwkeurigheid is 8 maal die van de atomaire afstand.
De Si-Si-bindingsenergie is 310 kJ/mol, dus je kunt begrijpen dat de bindingsenergie de kracht is die deze twee atomen uit elkaar trekt, en hoe groter de bindingsenergie, hoe groter de kracht die je nodig hebt om uit elkaar te trekken.
Si-atomen hebben bijvoorbeeld een grote diameter, wat overeenkomt met een appel, en C-atomen hebben een kleine diameter, wat overeenkomt met een sinaasappel, en een gelijk aantal sinaasappels en appels zijn op elkaar gestapeld om een SiC-kristal te vormen.
SiC is een binaire verbinding, waarbij de atoomafstand van de Si-Si-binding 3,89 A is. Hoe kunnen we deze afstand begrijpen? Momenteel heeft de meest uitstekende lithografiemachine op de markt een lithografienauwkeurigheid van 3 nm, wat een afstand is van 30A, en de lithografienauwkeurigheid is 8 maal die van de atomaire afstand.
De Si-Si-bindingsenergie is 310 kJ/mol, dus je kunt begrijpen dat de bindingsenergie de kracht is die deze twee atomen uit elkaar trekt, en hoe groter de bindingsenergie, hoe groter de kracht die je nodig hebt om uit elkaar te trekken.
We weten dat elke substantie uit atomen bestaat, en de structuur van een kristal is een regelmatige rangschikking van atomen, wat een lange-afstandsorde wordt genoemd, zoals de volgende. De kleinste kristaleenheid wordt een cel genoemd. Als de cel een kubieke structuur is, wordt deze een dicht opeengepakte kubus genoemd, en de cel een hexagonale structuur, wordt deze een dicht opeengepakte hexagonaal genoemd.
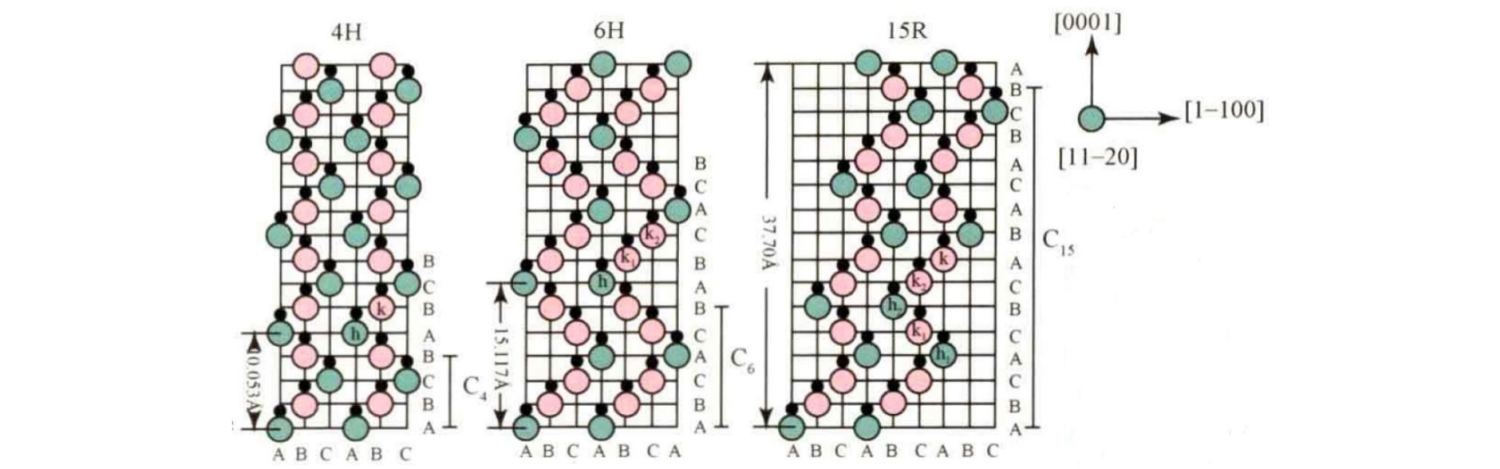
Veel voorkomende SiC-kristaltypen zijn onder meer 3C-SiC, 4H-SiC, 6H-SiC, 15R-SiC, enz. Hun stapelvolgorde in de richting van de c-as wordt weergegeven in de figuur.
Onder hen is de basisstapelvolgorde van 4H-SiC ABCB...; De basisstapelvolgorde van 6H-SiC is ABCACB...; De basisstapelvolgorde van 15R-SiC is ABCACBCABACABCB... .
Dit kan worden gezien als een steen voor het bouwen van een huis. Sommige huisstenen kunnen op drie manieren worden geplaatst, sommige kunnen op vier manieren worden geplaatst, sommige op zes manieren.
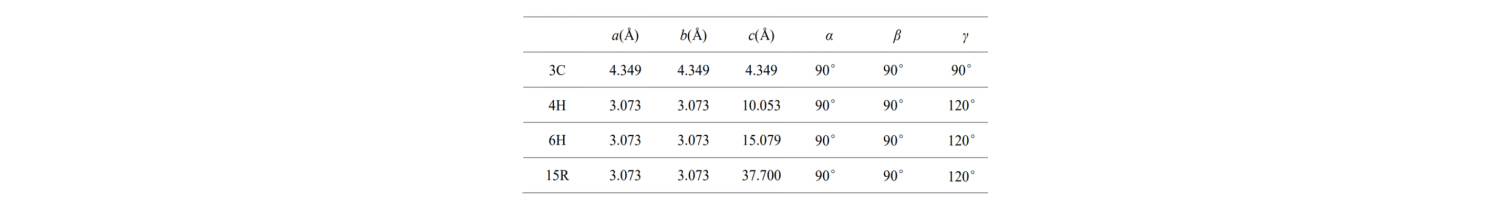
De basiscelparameters van deze veel voorkomende SiC-kristaltypen worden weergegeven in de tabel:
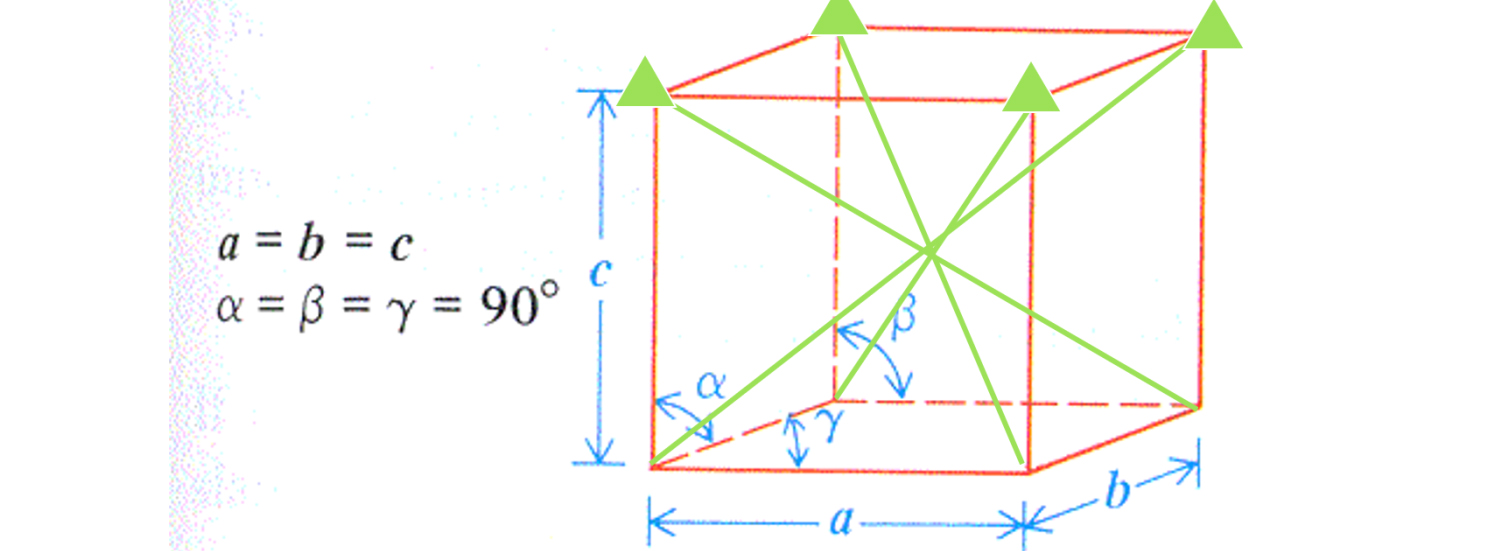
Wat betekenen a, b, c en hoeken? De structuur van de kleinste eenheidscel in een SiC-halfgeleider wordt als volgt beschreven:
In het geval van dezelfde cel zal de kristalstructuur ook anders zijn, dit is alsof we de loterij kopen, het winnende nummer is 1, 2, 3, je hebt 1, 2, 3 drie nummers gekocht, maar als het nummer gesorteerd is anders is het winnende bedrag anders, dus het aantal en de volgorde van hetzelfde kristal kan hetzelfde kristal worden genoemd.
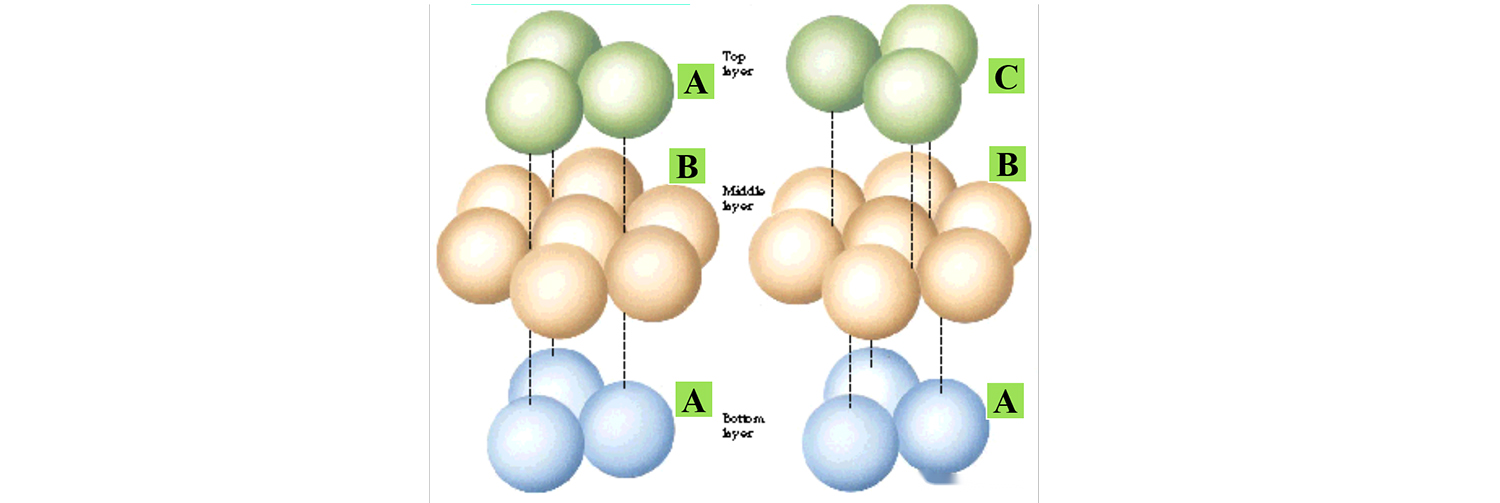
De volgende afbeelding toont de twee typische stapelmodi, alleen het verschil in de stapelmodus van de bovenste atomen, de kristalstructuur is anders.
De kristalstructuur gevormd door SiC is sterk gerelateerd aan de temperatuur. Onder invloed van hoge temperaturen van 1900 ~ 2000 ℃ zal 3C-SiC langzaam transformeren in een hexagonale SiC-polyvorm zoals 6H-SiC vanwege de slechte structurele stabiliteit. Juist vanwege de sterke correlatie tussen de waarschijnlijkheid van de vorming van SiC-polymorfen en de temperatuur, en de instabiliteit van 3C-SiC zelf, is de groeisnelheid van 3C-SiC moeilijk te verbeteren en is de bereiding moeilijk. Het hexagonale systeem van 4H-SiC en 6H-SiC is het meest gebruikelijk en gemakkelijker te bereiden, en wordt uitgebreid bestudeerd vanwege hun eigen kenmerken.
De bindingslengte van de SI-C-binding in SiC-kristal is slechts 1,89 A, maar de bindingsenergie is maar liefst 4,53 eV. Daarom is de energieniveaukloof tussen de bindingstoestand en de anti-bindingstoestand erg groot en kan er een brede bandafstand worden gevormd, die meerdere malen groter is dan die van Si en GaAs. De grotere bandbreedte betekent dat de kristalstructuur bij hoge temperaturen stabiel is. De bijbehorende vermogenselektronica kan de kenmerken van een stabiele werking bij hoge temperaturen en een vereenvoudigde warmtedissipatiestructuur realiseren.
De strakke binding van de Si-C-binding zorgt ervoor dat het rooster een hoge trillingsfrequentie heeft, dat wil zeggen een fonon met hoge energie, wat betekent dat het SiC-kristal een hoge verzadigde elektronenmobiliteit en thermische geleidbaarheid heeft, en dat de bijbehorende vermogenselektronische apparaten een hogere schakelsnelheid en betrouwbaarheid, waardoor het risico op uitval van te hoge temperaturen van het apparaat wordt verminderd. Bovendien zorgt de hogere doorslagveldsterkte van SiC ervoor dat het hogere doteringsconcentraties kan bereiken en een lagere aan-weerstand heeft.
Ten tweede de geschiedenis van de ontwikkeling van SiC-kristallen
In 1905 ontdekte Dr. Henri Moissan een natuurlijk SiC-kristal in de krater, dat op een diamant leek, en noemde het de Mosan-diamant.
Al in 1885 verkreeg Acheson SiC door cokes met silica te mengen en dit in een elektrische oven te verwarmen. Destijds dachten mensen dat het een mengsel van diamanten was en noemden het amaril.
In 1892 verbeterde Acheson het syntheseproces. Hij mengde kwartszand, cokes, een kleine hoeveelheid houtsnippers en NaCl, en verwarmde dit in een vlamboogoven tot 2700 ℃, en verkreeg met succes geschubde SiC-kristallen. Deze methode voor het synthetiseren van SiC-kristallen staat bekend als de Acheson-methode en is nog steeds de reguliere methode voor het produceren van SiC-schuurmiddelen in de industrie. Vanwege de lage zuiverheid van synthetische grondstoffen en het ruwe syntheseproces produceert de Acheson-methode meer SiC-onzuiverheden, slechte kristalintegriteit en kleine kristaldiameter, wat moeilijk is om te voldoen aan de eisen van de halfgeleiderindustrie voor grote, hoge zuiverheid en hoge -kwaliteitskristallen en kunnen niet worden gebruikt voor de vervaardiging van elektronische apparaten.
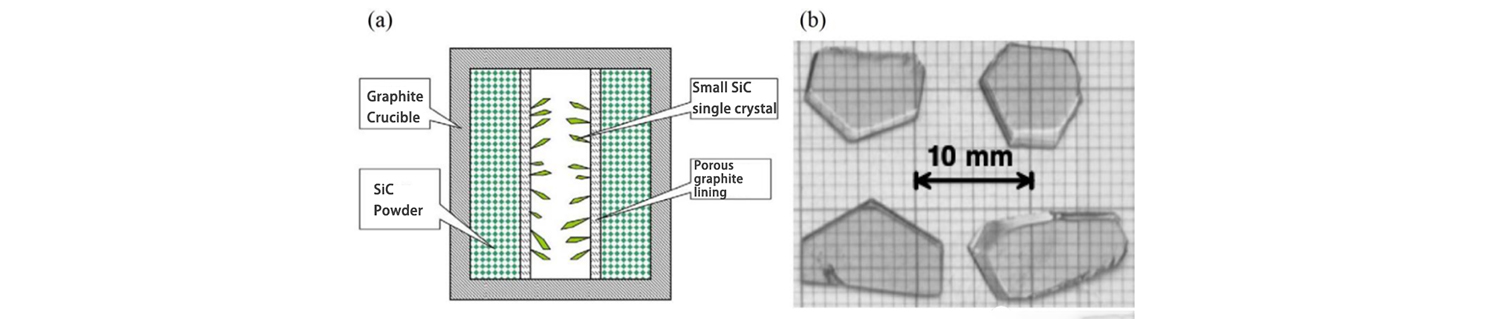
Lely van Philips Laboratory stelde in 1955 een nieuwe methode voor voor het kweken van SiC-kristallen voor. Bij deze methode wordt een grafietkroes gebruikt als groeivat, wordt SiC-poederkristal gebruikt als grondstof voor het kweken van SiC-kristal, en wordt poreus grafiet gebruikt om te isoleren. een hol gebied vanuit het midden van de groeiende grondstof. Tijdens het groeien wordt de grafietkroes verwarmd tot 2500 ℃ onder de atmosfeer van Ar of H2, en het perifere SiC-poeder wordt gesublimeerd en ontleed in Si- en C-dampfasestoffen, en het SiC-kristal wordt in het middelste holle gebied na het gas gegroeid. De stroom wordt door het poreuze grafiet overgebracht.
Ten derde, SiC-kristalgroeitechnologie
De monokristallijne groei van SiC is moeilijk vanwege zijn eigen kenmerken. Dit is voornamelijk te wijten aan het feit dat er geen vloeibare fase is met een stoichiometrische verhouding van Si: C = 1:1 bij atmosferische druk, en deze kan niet worden gekweekt met de meer volwassen groeimethoden die worden gebruikt door het huidige reguliere groeiproces van de halfgeleider. industrie - cZ-methode, vallende smeltkroesmethode en andere methoden. Volgens theoretische berekeningen kan alleen wanneer de druk groter is dan 10E5atm en de temperatuur hoger dan 3200 ℃ de stoichiometrische verhouding van Si: C = 1:1 oplossing worden verkregen. Om dit probleem te overwinnen hebben wetenschappers niet-aflatende pogingen ondernomen om verschillende methoden voor te stellen om SiC-kristallen van hoge kwaliteit, grote afmetingen en goedkope SiC-kristallen te verkrijgen. Momenteel zijn de belangrijkste methoden de PVT-methode, de vloeistoffasemethode en de dampchemische afzettingsmethode bij hoge temperatuur.
Posttijd: 24 januari 2024